Des Savants Fous Restructurent
Génétiquement Des Embryons Humains !
21 Juillet 2015
Pour la première fois, des scientifiques ont annoncé la modification génétique d'embryons humains (modification germinale), dans une étude menée par des chercheurs de l'Université Sun Yat-sen de Guangzhou, en Chine, et publiée dans la revue Protein & Cell (Protéines et Cellules).
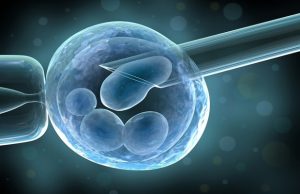
Auparavant, les scientifiques se limitaient à modifier les génomes des cellules adultes, en grande partie en raison de préoccupations éthiques et de préoccupations concernant les effets secondaires potentiels.
En effet, le nouvel article a conclu que la modification du génome des embryons se heurte toujours à de sérieux obstacles en matière de sécurité.
"Je pense qu'il s'agit du premier rapport de CRISPR/Cas9 appliqué aux embryons préimplantatoires humains et en tant que tel, l'étude est un point de repère, ainsi qu'un récit édifiant," a déclaré le chercheur en cellules souches George Daley de la Harvard Medical School, qui était pas impliqué dans la recherche. "Leur étude devrait être un avertissement sévère à tout praticien qui pense que la technologie est prête à être testée pour éradiquer les gènes de la maladie."
Taux de mutation incroyablement élevé
Afin de dissiper partiellement les préoccupations éthiques, l'expérience a été réalisée sur des embryons non viables obtenus auprès de cliniques de fertilité. Ces embryons ne pourraient jamais donner lieu à une naissance vivante, même s'ils étaient implantés.
Les chercheurs ont cherché à modifier le gène responsable d'un trouble sanguin potentiellement mortel connu sous le nom de s-thalassémie. Ils ont utilisé une technique d'édition de gènes appelée CRISPR/Cas9, qui a été utilisée avec succès pour modifier les génomes de cellules adultes dans le passé. La technique consiste à injecter aux cellules cibles le complexe enzymatique CRISPR/Cas9, programmé pour cibler (supprimer) un gène spécifique. En même temps, une autre molécule est injectée qui est programmée pour insérer un nouveau gène à la place de ceux qui ont été supprimés.
Les chercheurs ont injecté les molécules à 86
embryons humains unicellulaires, puis ont attendu 48 heures pour qu'ils se multiplient en environ huit cellules chacun. Seuls 71 embryons ont survécu au processus, et seulement 54 d'entre eux ont été génétiquement testés. Le gène d'origine a été supprimé avec succès dans seulement 24 cas, et dans seulement quelques-uns d'entre eux
le gène de remplacement a pris racine.
"Si vous voulez le faire dans des embryons normaux, vous devez être proche de 100%", a déclaré le chercheur principal Junjiu Huang. "C'est pourquoi nous avons arrêté. Nous pensons toujours que c'est trop immature."
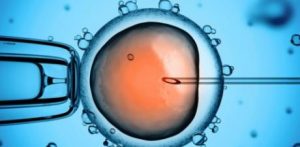
De plus, le processus a conduit à un nombre surprenant de mutations, causées par CRISPR/Cas9 ciblant la mauvaise partie du gène. Le taux de mutation était beaucoup plus élevé que celui observé dans les embryons de souris ou les cellules
humaines adultes.
Huang a averti que parce que seule une petite partie du génome a été testée, le taux de mutation était probablement encore plus élevé que celui rapporté.
Les scientifiques demandent un moratoire
L'article a été précédé pendant des mois par des rumeurs, qui ont conduit à un éditorial de mars dans la revue Nature, appelant à un moratoire sur la modification de la lignée germinale.
Les thérapies géniques existantes ne modifient les gènes que dans les cellules adultes et sont donc plus limitées dans leurs effets. Cela peut restaurer certaines fonctions d'un organe endommagé, par exemple, mais est moins susceptible de provoquer des changements majeurs dans d'autres types de cellules que la modification
de la lignée germinale.
En revanche, un œuf fécondé (zygote) finit par se multiplier et se différencier en chaque cellule de l'organisme adulte. La modification du génome de cette cellule entraîne des changements dans le génome à l'échelle de l'organisme et peut potentiellement modifier la fonction de chaque organe du corps. De plus, ces changements sont transmis aux générations futures, par définition sans leur consentement. Il est également impossible de comprendre pleinement les effets à long terme que ces modifications pourraient avoir, à travers les générations.

De nombreux éthiciens ont également averti que toute modification de la lignée germinale ouvre une pente glissante vers des tentatives "d'amélioration" du génome humain, telles que la création de "bébés sur mesure". Les utilisations de la modification de la lignée germinale sont si vastes que le risque d'utilisations contraires à l'éthique est énorme.
Cependant, d'autres études de modification de la lignée germinale sont déjà en cours ailleurs en Chine.
Liens Connexes :
* Researchers want to genetically modify humans in supposed “cure” for obesity
* Genetically
Modified Humans? Trying to Prevent Diseases Before They Start
* UK Scientists Apply For License to Genetically Modify Human Embryos
* Lab for genetic modification of human
embryos just $2,000 away
* Scientists call for urgent debate on
‘designer babies’ as GM technology advances
* UK scientists allowed to genetically modify human embryos – regulator
Scientists are Genetically Editing Human Beings in Labs and No One is Monitoring
Them
* The World Takes 4th Major Step Towards Creating GMO Babies in a Year
* Scientists generate a new type of human stem cell that has half a genome
* New Technology, Same Old Eugenics
* Designer Babies Could Remove The Need For Sex & End Genetic Diseases
* Chinese Researchers Experiment with Making HIV-Proof Embryos
* Protection Without a Vaccine
*
Japanese scientists given green light to modify fertilized human eggs
* Will Genetic Advances Make Sex Obsolete?
*
Scientists eye creating synthetic human genomes in lab
* The Future is Now! Chinese Scientists Pioneer Human Gene Editing
*
Scientists install ‘memories’ in DNA of human cells
* Genetic Manipulation – The New Weapon Of Mass Destruction
* World’s
first ‘3-person baby’ born using ‘revolutionary’ method
* Britain agrees to license three-parent IVF babies to prevent disease
* US experts approve creation of three-parent boys – but no girls allowed
* Scientists Want to Create Babies from DNA of 4 Parents
* Breaking Taboo, Swedish Scientist Seeks To Edit DNA Of Healthy Human Embryos
* Mad scientists to fall back on “CRISPR off switch” in case human gene
editing goes horribly wrong
* DNA editing to rid embyros of serious diseases takes step closer
* Designer Babies: Genetically Modified Humans Will Soon Walk Among Us
* First human embryo editing experiment in U.S. ‘corrects’ gene for heart
condition
* Where’d you get those genes? The answer may shock you
* Scientists build DNA from scratch to alter life’s blueprint
*
Genetic engineering ‘breakthrough’ could slow aging, reverse blindness
* New tech for controlling genetic inheritance and genome engineering